本文介绍的是中国科学院上海技术物理研究所郑伟波课题组、王少伟课题组以及上海市皮肤病医院王秀丽课题组共同研发的一种用于快速检测早期皮肤癌的小型荧光成像装置,发表在《Journal of Innovative Optical Health Sciences》期刊2021年第14期。
A miniaturized fluorescence imaging device for rapid early skin cancer detection
一种用于快速检测早期皮肤癌的小型荧光成像装置
Jingyue Pan, Qingquan Liu, Hao Sun, Weibo Zheng, Peiru Wang, Long Wen, Junli Duan, Zhiyi Xuan, Xiang Yu, Shaowei Wang, Xiuli Wang, Tao Zhang and Wei Lu
研究背景
皮肤癌是目前全球最常见的癌症之一,在白色人种中较为常见。近年来,随着参加户外活动的人数逐年增加以及环境污染等因素,中国皮肤癌患者也逐年增多。皮肤肿瘤位于身体浅表层,有2000多种细分类别,在临床上主要由两个大类组成,黑色素瘤(melanoma, MM)及非黑色素瘤(non-melanoma skin cancer, NMSC)。多数恶性黑色素瘤首先在原位呈现放射性生长,持续一段时间后转为生长迅速、致死率高的侵袭性生长。对于非黑色素肿瘤,其癌前病变有多种形态,包括日光性角化病(Actinic keratosis, AK)、鲍温样丘疹、皮角等。其中日光性角化病若不能及时治疗,则可能转为侵袭性鳞癌,并随淋巴转移至全身。因此,不管针对非黑色素肿瘤还是黑色素肿瘤,如果能对早期肿瘤或癌前病变进行及时诊断并及时治疗,绝大多数患者的皮肤肿瘤进程可得到控制。然而,早期皮肤肿瘤的特性并不明显,不易与正常皮肤区别,这导致一些常规的皮肤影像检测手段,如皮肤镜、反射式共聚焦显微镜等很难快速大规模查看疑似肿瘤的部位。
研究表明,皮肤肿瘤的代谢情况往往异常于正常组织,可以通过对肿瘤代谢物的特异性荧光标记区分早期皮肤肿瘤与正常组织。光敏剂介导荧光检测是利用特殊光敏剂药物激发荧光的检测方式,又称为光动力诊断(Photodynamic Diagnosis,PDD)。它用特定光敏剂外敷于皮肤病灶处,使光敏剂在肿瘤内部高浓度聚集,再使用特定波长照射,使肿瘤部位产生荧光,进而可根据荧光的边界对肿瘤边界做出诊断。然而目前的荧光成像设备存在体积大、照明不均匀、能耗高等问题,不仅限制了设备的使用条件,也限制了设备功能的拓展。
内容简介
本文巧妙地设计了一种具有同轴光路系统的荧光成像设备,其激发光和荧光位于同一光路中,这样不仅极大地减少了成像设备的体积,降低了使用的功率,同时解决了照明不均匀的问题。另外,我们在患有鳞状细胞癌 (squamous cell carcinoma)的小鼠身上进行皮肤癌荧光成像实验,实验结果表明该设备能够对早期皮肤肿瘤进行快速鉴别和成像。
图文导读
1.荧光肿瘤成像设备
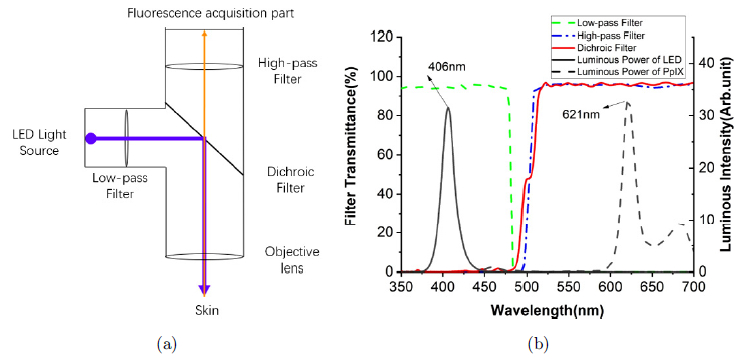
图1:荧光成像设备原理图。(a)成像光路;(b)高通滤光片、低通滤光片、二向色滤光片的透射率以及LED激发光、PpIX荧光光谱
如图1(a)所示,荧光成像设备主要由LED光源(激发光源)、荧光探测系统、低通滤光片、高通滤光片、二向色滤光片以及物镜组成。左侧的LED光源发出了蓝光通过低通滤光片,被二向色片反射,经过物镜最终照射在皮肤表面并激发红色荧光;荧光被物镜接收,依次经过二向色滤光片、高通滤光片最终到达荧光探测系统并成像。实验设备外观如图2所示,激发光源和探测部分一体化集成,整个装置尺寸仅3.5×3.5×9.5cm3, 重量150g,总功率只有1.5W。目前国际上采用的是激发光源和探测系统分立的荧光检测相机(Kulyket al, Photodiagn. Photodyn. Therapy 12, 630,2015),仅探测系统的体积就有108cm3、功率2W,再外加激光光源不仅增加了相机的体积、重量和功耗,还会导致操作不方便和照明不均匀等问题。


图2:荧光成像设备外观
2.实验对象
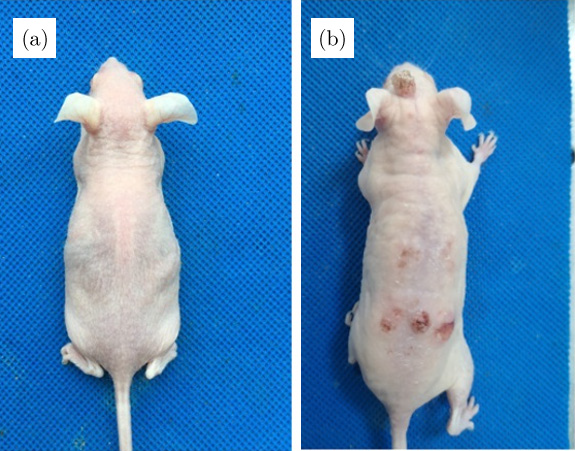
图3:无毛SKH-1小鼠照片。(a)对照组,(b)鳞状细胞癌小鼠
这里以无毛SKH-1小鼠作为实验对象。选择鳞状细胞癌小鼠两只作为实验组,健康的小鼠两只作为对照组。实验组中选择一只小鼠用浸润了10%ALA溶液的棉片外敷2小时,避光;另一只避光但不涂ALA溶液。在对照组中,选择一只在相同部位用相同的方法涂敷ALA溶液,避光;另一只避光但不涂ALA溶液。这里ALA是5-氨基乙酰丙酸(5- aminolevulinic acid)的简称,该药物是荧光试剂原卟啉IX(ProtoporphyrinIX, PpIX)的前体。
3.相机参数调节
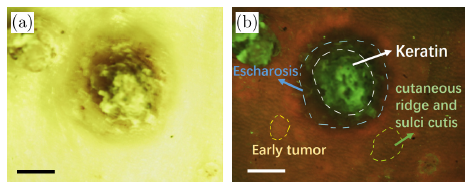
图4:恶性鳞状细胞癌肿瘤成像。(a)白光成像;(b)荧光成像。比例尺:2mm
实验取小鼠肉眼可见的恶性肿瘤病灶,在肿瘤病灶处用浸润了10%ALA溶液的棉片外敷2小时,避光。2小时后,取下ALA棉片,用麻醉机麻醉小鼠,将病灶部位置于荧光成像系统正下方,通过微调实验中相机的高度,保证荧光及白光成像效果,成像范围为1.2cm x 1.0cm。荧光图像拍摄时,关闭白光日光灯,只打开成像系统自带的405nmLED光源;拍摄白光图像时,关闭系统光源,打开白光日光灯。成像结果如图3所示。
4.早期肿瘤荧光成像
在完成荧光成像系统的参数调节以后,安排实验探究本荧光成像系统在早期肿瘤检测方面的应用效果。拍摄条件如下:取实验组中的小鼠与对照组的小鼠,在相同身体部位的定位区域,用10%ALA溶液浸润的棉片避光外敷2小时后,拍摄白光及荧光图像。实验组中的另外一只小鼠(Tumor-blank)与对照组中的另外一只小鼠(Control-blank),仅拍摄荧光及白光图像。与参数调节实验相同,荧光图像拍摄时,关闭白光日光灯,只打开成像系统自带的405nm LED光源;拍摄白光图像时,关闭系统光源,打开白光日光灯。
实验组的实验结果如图5所示,(a) 未涂ALA的白光成像;(b) 涂ALA的白光成像;(c) 未涂ALA的荧光成像;(d) 涂ALA的荧光成像。可以看出,在5(d)的荧光图像下,早期肿瘤部位呈现出比正常皮肤部位更强的砖红色荧光,能够明显地区分出。而在白光下,如5(b)所示,早期肿瘤部位与正常皮肤部位在颜色、纹理上及其相似,无法用肉眼区分正常皮肤与早期肿瘤部位。而对于未涂敷ALA的小鼠均无法辨认出肿瘤。

图5:实验组小鼠早期皮肤肿瘤的成像。(a)未涂ALA的白光成像;(b)涂ALA的白光成像;(c)未涂ALA的荧光成像;(d)涂ALA的荧光成像。比例尺:1mm
对照组的实验结果见图6,(a) 未涂ALA的白光成像;(b) 涂ALA的白光成像;(c) 未涂ALA的荧光成像;(d) 涂ALA的荧光成像。对于正常皮肤且涂敷ALA的小鼠,荧光图片中呈现出正常皮肤的纹路,包括淡红色的皮脊与黑灰色的皮沟,还有呈点状的凸起,见图6(d)。白光图像下只能呈现正常皮肤凸起等纹理,见图6(b)。对于正常皮肤且未涂敷ALA的小鼠(Control - blank)405nm光源下的荧光非常微弱,仅有成片点状的绿色荧光,见图6(c)。而白光图片则能较好的展示皮肤纹路,见图6(a)。
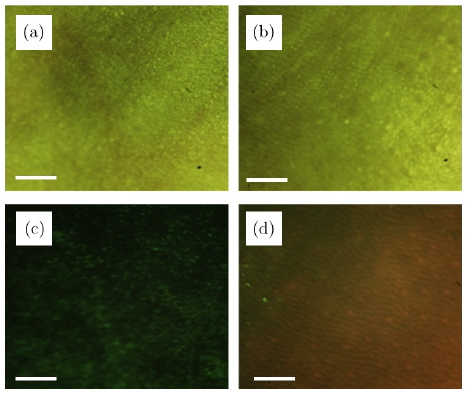
图6:对照组小鼠早期皮肤肿瘤的成像。(a)未涂ALA的白光成像;(b)涂ALA的白光成像;(c)未涂ALA的荧光成像;(d)涂ALA的荧光成像。比例尺:1mm。
由本实验可得出结论,本文中探讨的肿瘤荧光成像原理正确。利用荧光成像原理,本课题设计的小型化肿瘤荧光成像系统能成功的采集到早期肿瘤荧光图像,荧光图像中的肿瘤荧光能很好的区分正常皮肤与肿瘤区域。
通讯作者简介

王少伟,中国科学院上海技术物理研究所研究员,博士生导师,多项国家及省部级人才计划入选者,中国光学工程学会理事,国家重点研发计划重点专项、上海市科学技术奖等评审专家。长期从事微纳光子学器件方面的研究,包括超材料、超表面的光场调控,微腔光子学,分光芯片微型光谱探测技术,以及光谱技术的生物医学应用等。主持973和863等国家和省部级等项目二十余项,曾作为主要完成人荣获2014国家自然科学二等奖、2011国家技术发明二等奖、2012中国专利优秀奖、2010年度上海市技术发明一等奖、2007年度上海市自然科学一等奖,以及2019年度国际先进材料协会奖章(IAAM Medal)、2012年度“上海市科技系统青年五四奖章”、2009年度中国科学院卢嘉锡青年人才奖、2007年第六届饶毓泰基础光学奖等多项奖励与荣誉。发表Adv. Mater.和Nano Energy等SCI论文80余篇,他引1400余次,撰写Elsevier出版社《Modern Coating Technologies》手册等章节2个;获国家发明专利授权53项(其中美国1项)。是Elsevier出版社Microelectronics Engineering学术期刊副主编及Nature Electronics等审稿人,在SPIE等重要国际会议上作邀请报告或分会主席二十余次。
王秀丽

王秀丽教授,上海市皮肤病医院主任医师,复旦大学和德国慕尼黑大学双博士,同济大学教授、博导,同济大学医学院光医学研究所所长,享受国务院特殊津贴,现任国际光动力协会常务理事、中华医学会皮肤性病学分会光动力治疗研究中心首席专家、中国康复医学会皮肤病康复专业委员会候任主委、中华预防医学会皮肤病与性病学预防与控制专业委员会常委、上海市医学会激光医学分会主委等。牵头制订《氨基酮戊酸光动力疗法临床应用专家共识》《紫外线治疗皮肤病临床应用专家共识》,论文被《寻常性痤疮治疗指南》引用。主持国家自然科学基金、人事部回国留学人员基金等23项。发表学术论文230余篇,其中SCI论文110余篇;主编主译著作4部、参编参译11部;获省部级科技进步一等奖1项、二等奖2项、三等奖4项、其他上海医学三等奖1项、成果推广奖1项、科技成果奖1项,国家专利4项。主持国际会议9次,作为大会主席主办国际会议5次。